1、 定义
化学需氧量(COD),是在一定条件下,用一定的强氧化剂处理水样时所消耗的氧化剂的量,以氧的毫克/升表示。
在酸性条件下,用高锰酸钾将水样中的某些有机物及还原性物质氧化,反应后剩余的高锰酸钾,用过量的草酸钠还原,再以高锰酸钾标准溶液回滴过量的草酸钠,通过计算求出水样中所含有机物及还原性物质所消耗的高锰酸钾的量。
2、 仪器
2.1 量筒:100ml;
2.2 三角瓶:250ml 两个; 2.3 烧杯:200ml; 2.4 滴定管:25ml; 2.5 沸水浴装置;
3、 试剂
所用蒸馏水需加KMnO4重蒸馏。 3.1 H2SO4(1+3):取1体积比重1.84的浓硫酸慢慢加到盛有3体积水的烧杯中,摇匀后,滴加KMnO4溶液**溶液呈浅红色,若红色褪去应再补加**浅红色不褪为止,转入试剂瓶。 3.2 0.1mol/L KMnO4 溶液:溶解3.2克KMnO4于1.2L水中,煮沸0.5~1h,使体积减少到1L左右,放置过夜,用G-3号玻璃砂芯漏斗过滤后,滤液储存于棕色瓶中,避光保存。 3.3 0.01mol/L KMnO4 溶液:吸取100ml 0.1N KMnO4溶液于1000毫升容量瓶中,用水稀释**标线,混匀,储存于棕色瓶中,避光保存。
3.4 0.1000N Na2C2O4溶液:称取0.6705克在105℃烘1h并在干燥器中冷却的Na2C2O4,放入烧杯中,加水和25ml(1+3)硫酸**Na2C2O4全部溶解,移入100ml容量瓶,用水稀释**标线。
3.5 0.0100N Na2C2O4标准溶液:吸取10.00ml 0.1000N Na2C2O4标准溶液置于100毫升容量瓶,用水稀释**标线。 3.6 Ag2SO4
4、 步骤
4.1 样品取样量:排水(干净):100ml;
原水(严重污染):1ml(原水)+99ml(蒸馏水); 精炼排水:60ml(原水)+40ml(蒸馏水);
4.2 试样加入(1+3)H2SO410ml,摇匀。 4.3 加入Ag2SO4 1g(正常),样品中氯离子多时可适当增加。
4.4 用滴定管加入10ml(0.01mol/L)KMnO4溶液,摇匀,立即放入沸水浴中加热30分钟(从水浴重新沸腾起计时)。沸水浴液面要高于反应溶液的液面。
4.5 从沸水浴中取下锥形瓶,趁热用滴定管加入10ml(0.01 mol/L)Na2C2O4溶液,摇匀,立即用0.01 mol/L KMnO4溶液滴定**溶液呈微红色,记录消耗的KMnO4溶液的毫升数V1。
4.6 KMnO4溶液校正系数的测定:取步骤4.5滴定完毕的水样,用滴定管加入10ml(0.01 mol/L)Na2C2O4溶液,再用0.01 mol/L KMnO4溶液回滴**溶液呈微红色。记录相当于10ml(0.01 mol/L)Na2C2O4溶液的KMnO4溶液的毫升数V2,则KMnO4溶液的校正系数K=10/ V2。
4.7 若水样用蒸馏水稀释时,需另取100ml蒸馏水,按步骤4.2~4.5测定空白值,记录消耗的0.01 mol/L KMnO4溶液的毫升数V0。
5、 计算


1、 定义
化学需氧量(COD),是指在强酸并加热的条件下,用重铬酸钾作为氧化剂处理水样时所消化氧化剂的量,以氧的mg/L来表示。化学需氧量反应了水中受还原星物质污染的程度,水中还原性物质包括有机物、亚硝酸盐、亚铁盐、硫化物等。水被有机物污染是很普遍的,因此化学需氧量也作为有机物相对含量的指标之一,但只能反映能被氧化的有机物污染,不能反映多环芳烃、PCB,二恶英等的污染状况。CODcr是我*实施排放总量的控制指标之一。
水样的化学需氧量,可由于加入氧化剂的种类及浓度,反应溶液的酸度,反应温度和时间,以及催化剂的有无而获得不同的结果。因此,化学需氧量亦是一个条件性指标,必须严格按照操作步骤进行。
对于污水,我*规定用重铬酸钾法,其测得的值称为化学需氧量。*外也有用高锰酸钾、臭氧、羟基作氧化剂的方法体系。如果使用,必须与重铬酸钾法做对照实验,做出相关系数,以重铬酸钾法上报检测数据。
2、 原理
在强酸性溶液中,用一定量的重铬酸钾氧化水样中还原性物质,过量的重铬酸钾以试亚铁灵作指示剂,用硫酸亚铁铵溶液回滴。根据硫酸亚铁铵的用量计算出水样中的还原性物质消耗氧的量。
3、 干扰及消除
酸性重铬酸钾氧化性很强,可氧化大部分有机物,加入硫酸银作催化剂时,直链脂肪族化合物可完全被氧化,而芳香族化合有机物却不易被氧化,吡啶不被氧化,挥发性直链脂肪族化合物、苯等有机物存在于蒸气相,不能与氧化剂液体接触,氧化不明显。氯离子能被重铬酸盐氧化,并且能与硫酸银作用产生沉淀,影响测定结果,故在回流前向水样中加入硫酸汞,使成为络合物以消除干扰。氯离子含量高于1000mg/L的样品应先作定量稀释,使含量降低**1000mg/L以下,再行测定。
4、 方法的适用范围
用0.25mol/L浓度的重铬酸钾溶液可测定大于50mg/L的COD值,未经稀释水样的测定上限是700mg/L,用0.025mol/L浓度的重铬酸钾溶液可测定5~50mg/L的COD值,但低于10mg/L时的测量准确度较差。
5、 试剂
5.1重铬酸钾标准溶液(1/6K2CrO7=0.2500mol/L);称取预先在120℃烘干2h的基准或优级纯重铬酸钾12.258g溶于水中,移入1000ml容量瓶,稀释**标线,摇匀。 5.2试亚铁灵指示液:称取1.458g邻菲啰啉(C12H8N2·H2O,1,10-phenanthroline),0.695g硫酸亚铁(FeSO4·7H2O)溶于水中,稀释**100ml,贮于棕色瓶内。 5.3硫酸亚铁铵标准溶液〔(NH4)2Fe(SO4)2·6H2O≈0.1mol/L〕:称取39.5g硫酸亚铁铵溶于水中,边搅拌边缓慢加入20ml浓硫酸,冷却后移入1000ml容量瓶中,加入稀释**标线,摇匀。临用前,用重铬酸钾标准溶液标定。 #p#分页标题#e#
5.3.1标定硫酸亚铁铵方法:准确吸取10.00ml重铬酸钾溶液于500ml锥形瓶中,加水稀释**110ml左右,缓慢加入30ml浓硫酸,混匀。冷却后,加入3滴试亚铁灵指示剂(约0.15ml),用硫酸亚铁铵溶液滴定,溶液的颜色由黄色经蓝绿色**红褐色即为终点。

5.4硫酸-硫酸银溶液:于2500ml浓硫酸中加入25g硫酸银。放置1~2d,不时摇动使其溶解(如无2500ml容器,可在500ml浓硫酸中加入5g硫酸银)。 5.5硫酸汞:结晶或粉末。
6、 步骤
6.1 取20.00ml混合均匀水样(或适量水样稀释**20.00ml)置250ml磨口的回流锥形瓶中,准确加入10.00ml重铬酸钾溶液及数粒洗净的玻璃珠或沸石,连接磨口回流冷凝管,从冷凝管上口慢慢的加入30ml硫酸-硫酸银溶液,轻轻摇动锥形瓶使溶液混匀,加热回流2h(自开始沸腾时计时)。
注:①对于化学需氧量高的废水样,可先取上述操作所需体积1/10的废水样和试剂,与15mm×150mm硬质玻璃试管中,摇匀,加热后观察是否变为绿色。如溶液显绿色,再适当减少废水取样量,知道溶液不变绿色为止,从而确定废水样分析时应取用的体积。稀释时,所取废水样不得少于5ml,如果化学需氧量很高,则废水样应多次逐级稀释。
②废水中氯离子含量超过30mg/L时,应先把0.4g硫酸汞加入回流锥形瓶中,再加20.00ml废水(或适量废水稀释**20.00ml)、摇匀。以下操作同上。
6.2 冷却后,用90ml水从上部慢慢冲洗冷凝管管壁,取下锥形瓶。溶液总体积不得少于140ml,否则因酸度太大,滴定终点不明显。
6.3 溶液再度冷却后,加3滴试亚铁灵指示液,用硫酸亚铁铵标准溶液滴定,溶液的颜色由黄色经蓝绿色**红褐色即为终点,记录硫酸亚铁铵标准溶液的用量。
6.4 测定水样的同时,以20.00ml重蒸馏水,按同样操作步骤作空白试验。记录滴定空白时硫酸亚铁铵标准溶液的用量。

汞 : 氯离子=10:1。若出现少量的氯化汞沉淀,并不影响测定。
8.2 水样用体积可在10.00~50.00ml范围之间,但试剂用量及浓度需按下表进行相应调整,也可得到满意的结果。
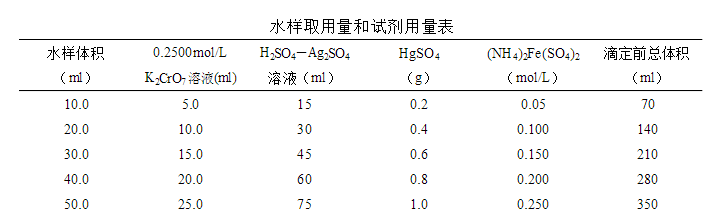
8.3 对于化学需氧量小于50mg/L的水样,应改用0.0250mol/L重铬酸钾标准溶液。回滴时用0.01mol/L硫酸亚铁铵标准溶液。
8.4 水样加热回流后,溶液中重铬酸钾剩余量应是加入量的1/5~4/5为宜。 8.5 用临苯二甲酸氢钾标准溶液检查试剂的质量和操作技术时,由于每克临苯二甲酸氢钾的理论CODCr为1.176g,所以溶解0.4251g临苯二甲酸氢钾(HOOCC6H4COOK)于重蒸馏水中,转入1000ml容量瓶,用重蒸馏水稀释**标线,使之成为500mg/L的CODCr标准溶液。用时新配。
8.6 CODCr的测定结果应保留三位有效数字。
8.7 每次实验时,应对硫酸亚铁铵标准滴定溶液进行标定,室温较高时尤其应注意其浓度的变化。标定方法亦可采用如下操作:于空白试验滴定结束后的溶液中,准确加入10.00ml、0.2500mol/L重铬酸钾溶液,混匀,然后用硫酸亚铁铵溶液进行标定。
8.8 回流冷却管不能用软质乳胶管,否则容易老化、变形、冷却水不通畅。 8.9 用手摸冷却水时不能有温感,否则测定结果偏低。
8.10 滴定时不能激烈摇动锥形瓶,瓶内试液不能溅出水花,否则影响测定结果。
1、定义
化学需氧量(COD),是在一定条件下,用一定的强氧化剂处理水样时所消耗的氧化剂的量,以氧的毫克/升表示。
1、 仪器
DRB200型数字式反应器(HACH) 2、 试剂
COD消解试剂瓶(0~150mg/L)
3、 步骤
4.1将试样样品搅拌均匀。
4.2开启COD分解炉,预热**150℃。
4.3根据样品的CONC的范围,选择适当的COD消解试剂瓶,打开瓶盖。 4.4向试剂瓶内加2ml试样。
4.5将试剂瓶放回原位。擦干净瓶外壁。
4.6扭紧试剂瓶盖。反转瓶多次,使溶液混合。将试剂瓶放上预热的COD反应器上。 4.7按照步骤4.3~4.6准备空白试样。用去离子水2ml代替样品。 4.8将所有试剂瓶加热2小时。
4.9关闭反应器。等待大约20分钟,等到试瓶温度低于120℃或以下。 4.10趁热反转试瓶多次。将瓶放在架上。等到其温度降**室温。(当绿色显现是,检测COD。如有必要,重复检测稀释的样品。)
4、 比色检测
5.1输入检测需氧量法的程序编号。按下:PRGM。屏幕显示:PRGM?
5.2按下:1,6键后,按下ENTER键,屏幕将显示:mg/L,COD和ZERO图标。(如果检测其他形态(O2),按下CONC键)
5.3旋转COD/TNT适配器,将其嵌入瓶管架上适当的位置,然后下按使之安全嵌入。 5.4用卫生纸擦净装有空白试样的试瓶。
5.5旋转COD/TNT配器,将其嵌入瓶管架上适当的位置,然后下按使之完全嵌入。 5.6盖紧瓶盖。
5.7按ZERO,指针将右移,屏幕显示:0mg/L COD。 5.8先用湿毛巾擦试剂样品瓶,擦去指纹或其它痕迹。 5.9将药品试剂放入样品配器中。 5.10盖紧瓶盖。 #p#分页标题#e#
5.11按下:READ指针将右移,屏幕将显示COD的含量,单位是mg/L。1、 定义
化学需氧量(COD),是在一定条件下,用一定的强氧化剂处理水样时所消耗的氧化剂的量,以氧的毫克/升表示。
2、 仪器
2.1 量筒:100ml;
2.2 三角瓶:250ml 两个; 2.3 烧杯:200ml; 2.4 滴定管:25ml; 2.5 沸水浴装置;
3、 试剂
3.1 硫酸(1+2)
3.2 0.005mol/L KMnO4溶液:0.790gKMnO4/L
3.3 0.0125 mol/L Na2C2O4标准溶液:1.675gNa2C2O4/L 3.4 Ag2SO4
4、步骤
4.1 样品取样量:排水(干净):100ml;
原水(严重污染):1ml(原水)+99ml(蒸馏水); 精炼排水:60ml(原水)+40ml(蒸馏水);
4.2 试样加入(1+2)H2SO410ml,摇匀。 4.3 加入Ag2SO4 1g(正常),样品中氯离子多时可适当增加。
4.4 用滴定管加入10ml(0.005mol/L)KMnO4溶液,摇匀,立即放入沸水浴中加热30分钟。沸水浴液面要高于反应溶液的液面。
4.5 从沸水浴中取下锥形瓶,趁热用滴定管加入10ml(0.0125 mol/L)Na2C2O4溶液,摇匀,立即用0.005 mol/L KMnO4溶液滴定**溶液呈微红色,记录消耗的KMnO4溶液的体积数a。 4.6 空白试验同时进行,消耗KMnO4溶液的体积数b。